高中化学知识点:天然气的综合利用
逍遥学能 2017-01-09 21:27
天然气的综合利用:
(1)主要成分是CH4,是一种清洁的化石燃料和重要的化工原料。
(2)用途:合成NH3和CH3OH。
以甲烷、水和空气制NH,的化学方程式为: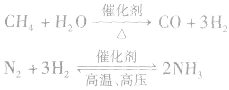
相关高中化学知识点:验证物质燃烧的条件
定义:
燃烧是一种发光、发热的剧烈的化学反应。认识燃烧,科学地利用和控制燃烧,使燃烧为人类服务是十分重要的。
燃烧条件的探究实验:
1. 实验方案
| 实验方案 | 实验现象 | 分析 |
分别将一小块白磷和一小块红磷放在薄铜片上,另取一小块白磷放入热水中,如下图: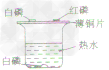 | ①薄铜片上:白磷燃烧,产生大量白烟,红磷没有变化 ②热水中,白磷没有燃烧 | ①白磷、红磷都是可燃物.薄铜片上的白磷与O2接触,同时温度达到白磷的着火点,故白磷能够燃烧 ②薄铜片上的红磷与O2 接触,但温度没有达到其着火点,热水中的白磷温度达到了其着火点.但没有与O2接触,所以红磷和水中的白磷都不能燃烧 |
2. 实验结论:
燃烧必须同时具备:
①可燃物
②氧气(空气)
③达到燃烧所需的最低温度(着火点)
1. 着火点:可燃物燃烧所需的最低温度叫着火点,是物质固有的一种性质,与物质本身的性质有关,一般不随外界条件的改变而改变。
在通常状况下一些常见物质的着火点
| 物质 | 白磷 | 红磷 | 木材 | 木炭 | 无烟煤 |
| 着火点/℃ | 40 | 240 | 250-330 | 320-370 | 700-750 |
燃烧必须同时具备: ①可燃物 ②氧气(空气) ③达到燃烧所需的最低温度(着火点)。中考试题往往以实验设计题的形式来考查燃烧规律。燃烧条件的探究设计常常运用控制变量―对比法。
(1)分析对比实验设计
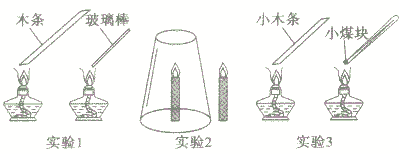
实验1:探究可燃物才能燃烧
实验2:探究可燃物接触氧气才能燃烧
实验3:探究达到着火点可燃物才能燃烧
(2)综合控制变量
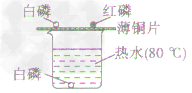
①把白磷和红磷都漏置在空气中(对比),用0℃的热水控制温度(这个温度高于白磷的着火点,低于红磷的着火点),白磷能燃烧,红磷不能燃烧,证明可燃物与氧气接触,且可燃物还必须达到着火点才能燃烧。
②烧杯底部放一块白磷,用水控制不让白磷与空气接触,温度仍然是80℃,与铜片上的白磷对比,证明可燃物即使温度达到着火点,如果不与氧气接触也不能燃烧。
版权声明:本文内容由互联网用户自发贡献,该文观点仅代表作者本人。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如发现本站有涉嫌抄袭侵权/违法违规的内容,请发送邮件至 lxy@jiyifa.cn 举报,一经查实,本站将立刻删除。